-1价 2?MgO2?
2MgO+O2↑ 放热 取少量煅烧后的固体,滴入稀盐酸,无气泡产生 防止过氧化氢受热分解或防止过氧化镁受热分解 650 2 700℃时,生成的氧化镁颗粒的表面积减小,与过氧化氢反应不充分 作过氧化氢分解的催化剂 80% BD
解析:
[分析]
[详解]
(1)过氧化镁中镁显+2价,设有元素的化合价为x,则+2+2x=0,的x=-1,故过氧化镁中氧元素的化合价为-1;过氧化镁有强氧化性,常温下比较稳定,但是加热时会分解生成氧气和氧化镁,该反应的化学方程式为:
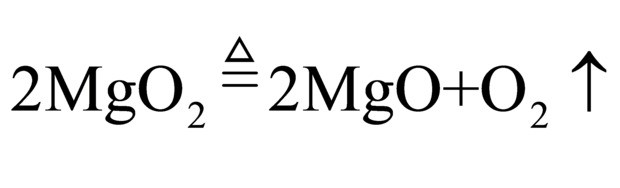
;
(2)过氧化镁易溶于稀盐酸,发生反应:MgO2+2HCl=MgCl2+H2O2同时温度升高,说明该反应放出热量;
(3)检测煅烧过程碱式碳酸镁完全分解的方法是:取少量煅烧后的固体,滴入稀盐酸,无气泡产生;上述生产过程加入稳定的剂的作用是:防止过氧化氢受热分解或防止过氧化镁受热分解。
(4)根据图1和图2,碱式碳酸镁煅烧的温度适宜控制在650℃,煅烧的时间适宜控制在2h。
(5)在适宜的温度和时间下,碱式碳酸镁能完全分解,并且得到的氧化镁颗粒表面积最大,能与30%过氧化氢充分反应,所以产率高。推测700℃时,产率明显降低的可能的原因是:700℃时,生成的氧化镁颗粒的表面积减小,与过氧化氢反应不充分。
(6)稀盐酸中放入的少量硫酸铜溶液目的是:作过氧化氢分解的催化剂;
(7)设过氧化镁的质量为x,反应后刻度管数为122mL,故生成氧气的体积为122mL-10mL=112mL,由MgO2+2HCl=MgCl2+H2O2,2H2O2

2H2O+O2↑得:
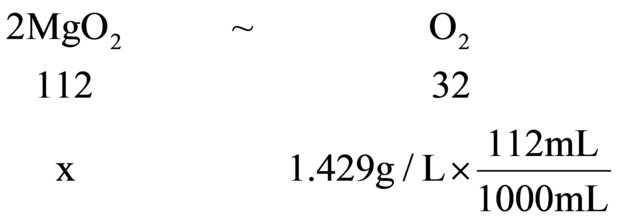
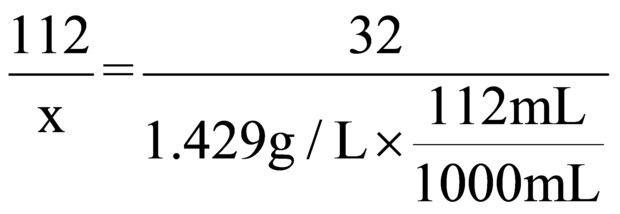
X=0.56g
所以样品中过氧化镁 的质量分数为
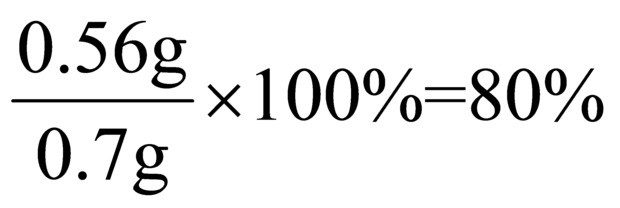
;
(8)该胡爱口行尼素古个罗小组同学所测得质量分数比实际结果偏大,你觉得可能的原因是:
A、生成的氧气有少量溶于水,会使氧气体积偏小 ,导致测量结果偏小;
B、未等装置冷却到室温就开始读数,气体受热膨胀,会使氧气体积偏大,过氧化镁质量增大 ,故样品中过氧化镁质量分数偏大 ;
C、杂质与盐酸能反应,会使测量结果偏小;
D、滴入的稀盐酸占了一部分气体的体积,会使氧气体积偏大 ,导致测量结果偏大。故选BD。
 2MgO+O2↑ 放热 取少量煅烧后的固体,滴入稀盐酸,无气泡产生 防止过氧化氢受热分解或防止过氧化镁受热分解 650 2 700℃时,生成的氧化镁颗粒的表面积减小,与过氧化氢反应不充分 作过氧化氢分解的催化剂 80% BD
2MgO+O2↑ 放热 取少量煅烧后的固体,滴入稀盐酸,无气泡产生 防止过氧化氢受热分解或防止过氧化镁受热分解 650 2 700℃时,生成的氧化镁颗粒的表面积减小,与过氧化氢反应不充分 作过氧化氢分解的催化剂 80% BD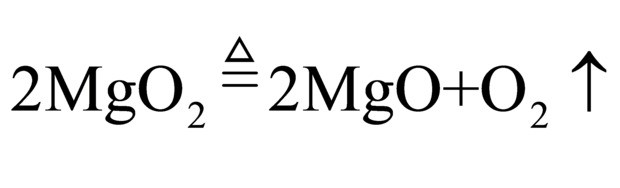 ;
; 2H2O+O2↑得:
2H2O+O2↑得:
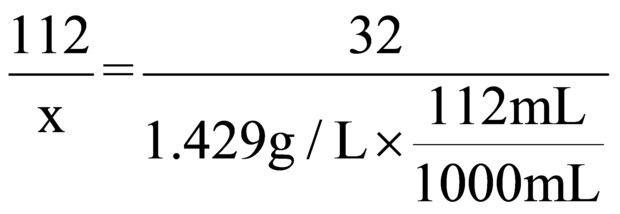
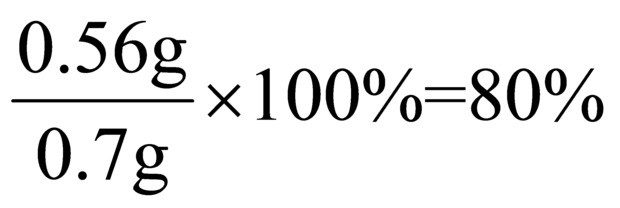 ;
;